近日,我校藥學院韓峰教授課題組、基礎醫學院盧應梅教授課題組以及蔣建東院士團隊合作在《細胞死亡和分化》(Cell Death & Differentiation)期刊在線發表了題為《內皮細胞源性SEMA3G通過誘導c-Myc降解抑制膠質母細胞瘤干細胞》(Endothelial cells-derived SEMA3G suppresses glioblastoma stem cells by inducing c-Myc degradation)的研究論文,闡明了內皮細胞來源的SEMA3G通過誘導關鍵標志物c-Myc的降解,進而破壞GSCs干性維持內在驅動力的分子機制。這一研究揭示了SEMA3G-c-Myc軸對膠質母細胞瘤微環境中細胞間通訊的擾動作用,為膠質瘤的靶標發現提供了新的研究思路。

膠質母細胞瘤特征性的異常血管新生不僅為腫瘤提供營養和氧氣支持,更構成了獨特的腫瘤微環境。膠質母細胞瘤干細胞(Glioblastoma stem cells,GSCs)傾向于定位于血管周圍微環境,通過與內皮細胞的復雜雙向互作維持其干性特征。深入探究血管內皮細胞與GSCs間細胞通訊的關鍵分子及其調控網絡,將為膠質母細胞瘤的新靶標發現提供重要的理論依據和新策略。
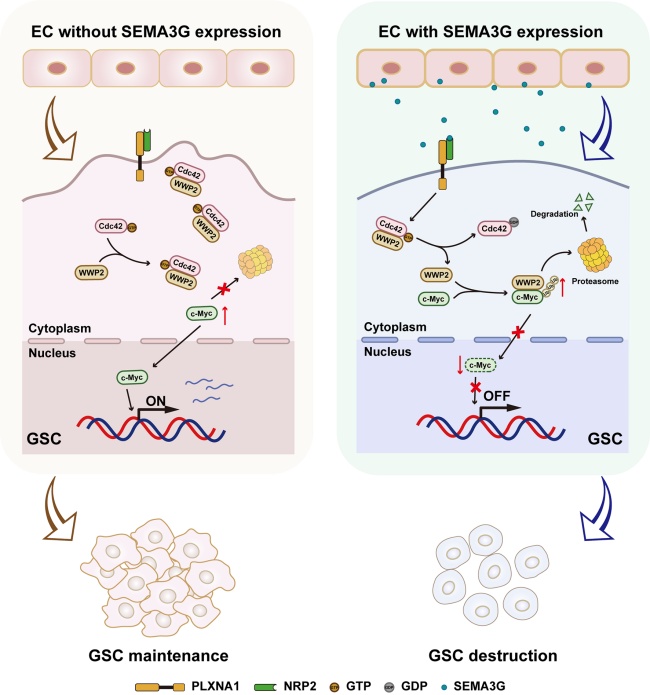
本研究從腦血管內皮細胞視角出發,通過整合分析多組公共數據集以及膠質母細胞瘤患者樣本,發現內皮細胞特異性表達的SEMA3G可能通過細胞間互作機制參與膠質母細胞瘤進展。動物實驗結果顯示,內皮細胞特異性Sema3G缺失促進膠質母細胞瘤的生長并縮短荷瘤小鼠的生存期。反之,SEMA3G重組蛋白則抑制腫瘤進展并延長小鼠生存其期。進一步的機制研究表明,SEMA3G通過作用于GSC的NRP2/PLXNA1受體復合物特異性抑制Cdc42-GTP活性。而失活狀態的Cdc42與E3泛素連接酶WWP2的結合偏好性減弱,促使WWP2與c-Myc結合并引起c-Myc的泛素-蛋白酶體途徑降解,導致GSC干性遭到破壞。本研究在國際上首次系統闡明腦血管內皮源性SEMA3G通過NRP2/PLXNA1-Cdc42-WWP2-c-Myc級聯信號軸調控GSC干性的分子機制,具有重要科學價值,為開發針對膠質母細胞瘤干細胞微環境的精準治療策略提供了候選新靶點。
我校藥學院韓峰教授、基礎醫學院盧應梅教授以及中國醫學科學院蔣建東院士為本論文共同通訊作者。南京醫科大學常州醫學中心博士后閔鵬翔、藥學院講師馮黎黎為共同第一作者。本項目在實施過程中得到南京醫科大學汪秀星教授等專家的支持和幫助。
本研究得到國家重點研發計劃等項目的資助。
原文鏈接:https://www.nature.com/articles/s41418-025-01534-3
(撰稿/閔鵬翔 馮黎黎;審核/韓峰)

