近日,基礎醫學院生理學系心血管實驗室朱國慶教授團隊在《細胞外囊泡雜志》(Journal of Extracellular Vesicles)發表了題為《自發性高血壓大鼠外膜成纖維細胞來源的外泌顆粒通過轉運骨橋蛋白促進血管重構》(Exomeres from adventitial fibroblasts of spontaneously hypertensive rats promote vascular remodelling via transferring osteopontin)的研究論文,發現自發性高血壓大鼠的血管外膜成纖維細胞釋放外泌顆粒(exomeres,EMs),通過轉運骨橋蛋白激活整合素αVβ3/FAK/PI3K/AKT信號通路,促進血管平滑肌細胞增殖和遷移,促進血管重構和加重高血壓,表明自發性高血壓大鼠的血管外膜成纖維細胞釋放的EMs在高血壓和血管重構中起重要作用,干預血管的骨橋蛋白和EMs可能是減輕高血壓血管重構的潛在治療策略。

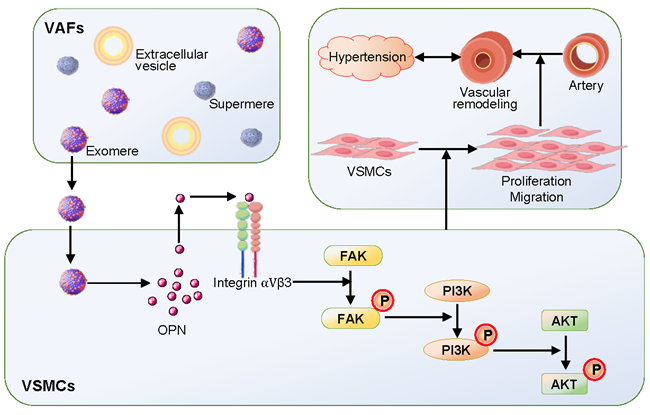
EMs和超微顆粒(supermeres,SMs)是近年來新發現的2種具有重要的細胞間通訊功能的非囊泡性細胞外納米顆粒(NVEPs),EMs和SMs不同于細胞外囊泡(extracellular vesicles,EVs),沒有脂質雙分子層膜包裹,且顆粒直徑更小。NVEPs的心血管病理生理學作用和機制尚不明確。本研究在前期探討EVs在高血壓血管重構中的作用與機制的基礎上,首次從血管外膜成纖維細胞中分離出EMs和SMs,并對EVs、EMs和SMs的特征進行比較和鑒定,發現自發性高血壓大鼠血管外膜成纖維細胞釋放的EMs在血管平滑肌細胞增殖和遷移、血管重構和高血壓發病機制中起重要作用,并揭示了其通過轉運骨橋蛋白激活下游整合素αVβ3/FAK/PI3K/AKT信號通路的重要機制,發現敲降動脈的骨橋蛋白減輕高血壓動物對應部位的血管重構,而長期靜脈注射SHR的EMs可加重血管重構和高血壓,EMs和骨橋蛋白是干預高血壓血管重構的重要靶點,該研究為防治高血壓血管重構提供了新的理論依據、實驗基礎和策略。
我校基礎醫學院生理學系朱國慶教授和熊曉青副教授為本論文共同通訊作者,王靜曉博士為本論文第一作者。本研究得到國家自然科學基金、江蘇省研究生科研與實踐創新計劃、江蘇省心血管病轉化醫學協同創新中心等資助。
原文鏈接:
https://isevjournals.onlinelibrary.wiley.com/doi/10.1002/jev2.70146
(供稿/朱國慶課題組;審核/陳峰 王覺進)

